研究盐酸被MnO2氧化. 实验 | 操作 | 现象 | I | 常温下将MnO2和12mol•L﹣1浓盐酸混合 | 溶液呈浅棕色,略有刺激性气味 | II | 将 I中混合物过滤,加热滤液 | 生成大量黄绿色气体 | III | 加热MnO2和4mol•L﹣1稀盐酸混合物 | 无明显现象 |
①已知MnO2呈弱碱性. I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,化学方程式是. ②II中发生了分解反应,反应的化学方程式是. ③III中无明显现象的原因,可能是c(H+)或c(Cl﹣)较低,设计实验(图1)IV进行探究: 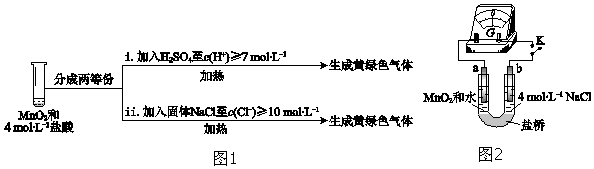
将实验 III、IV作对比,得出的结论是;将 i、ii作对比,得出的结论是. ④用图2装置(a、b均为石墨电极)进行实验 V: ⅰ.K闭合时,指针向左偏转 ⅱ.向右管中滴加浓H2SO4至c(H+)≥7mol•L﹣1 , 指针偏转幅度变化不大 ⅲ.再向左管中滴加浓H2SO4至c(H+)≥7mol•L﹣1 , 指针向左偏转幅度增大 将ⅰ和ⅱ、ⅲ作对比,得出的结论是. |