8.
请你参与某学习小组的探究活动,并回答相关问题: [发现问题]王馨悦同学发现盛水的铁锅在与水面接触的部位最易生锈;程后乐同学发现自己的铜制眼框表面出现了绿色的铜锈;顾浩宇同学发现苹果切开不久,果肉上会产生一层咖啡色物质,好象生了“锈”一般.
[提出问题]这三种物质“生锈”的原因是什么?
[收集证据]回忆已有知识:铁生锈的实质是铁与发生反应.
[查阅有关资料]“铜锈”主要成分是Cu2(OH)2CO3(俗称铜绿);苹果“生锈”是果肉里的物质(酚和酶)与空气中的氧气发生了一系列的反应,生成咖啡色的物质.碱石灰能吸水与二氧化碳.
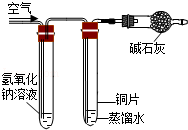
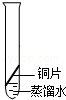
[实验探究]将四小块铜片分别按下图所示放置较长时间,观察现象如下:
实验装置 | 
| 
| 
| 
|
实验现象 | 铜片不生锈 | 铜片不生锈 | 铜片不生锈 | 铜片生锈且水面附近锈蚀最严重 |
由实验可知,铜生锈是铜与水、、等物质共同作用的结果.这个反应的化学方程式
为属反应.
[得出结论]三位同学认为这些物质“生锈”除了可能与水有关外,还可能都与(填物质名称)有关.
[反思与应用]利用所得结论填空:写出一种防止铁或铜等金属制品生锈的具体方法;请你提出一条延长食品保质期的建议.