| Ⅲ.用废锂电池制备 资料二:2Al+2NaOH+2H2O═2NaAlO2+3H2↑ 用废锂电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)制备纳米MnO2 , 并进行锂资源回收,流程如下: 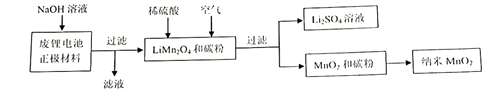
请回答下列问题: ( 1)“滤液”中溶质的主要成分是(填化学式). ( 2)在实验室进行“过滤”操作时,需要的玻璃仪器有烧杯、漏斗和. ( 3)MnO2与碳粉经下列三步反应制得纳米MnO2: ①2MnO2+C  2MnO+CO2↑ 2MnO+CO2↑ ②MnO+H2SO4═MnSO4+H2O ③3MnSO4+2KMnO4+2H2O═5MnO2↓+K2SO4+2H2SO4 上述涉及元素化合价变化的反应有(填序号). |