| 工业上常用CuSO4溶液、氨水和Na2S2O3溶液为原料配制浸金液,其一种可能的浸金原理示意图如下。
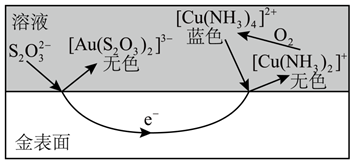 ①上述原理可知,[Cu(NH3)4]2+在浸金过程中起作用。 ②为了验证上述原理中O2的作用,进行如下实验。 实验现象:反应一段时间后,温度无明显变化,U形管内液柱左高右低,锥形瓶中溶液蓝色变浅,打开瓶塞后…… 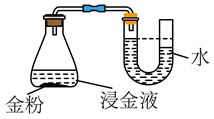 a.打开瓶塞后,(填实验现象),证实了上述原理。 b.a中现象对应反应的离子方程式是。 ③下图表示相同时间内,配制浸金液的原料中c(CuSO4)对浸金过程中  消耗率和浸金量的影响(其他条件不变)。 消耗率和浸金量的影响(其他条件不变)。 已知:2Cu2++6  ⇌2[Cu(S2O3)2]3-+ ⇌2[Cu(S2O3)2]3-+  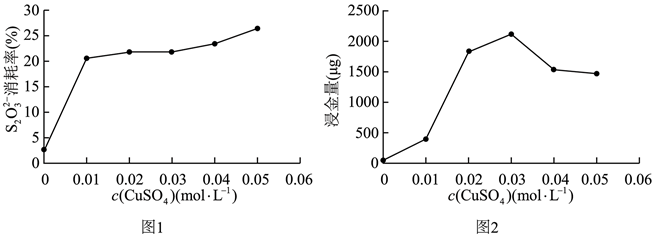 结合图1,解释图2中浸金量先上升后下降的原因:。 |