Ⅰ(经典赏析)教材介绍了拉瓦锡用定量的方法研究了空气的成分,实验装置及资料如下。
|
汞(有毒)
|
氧化汞
|
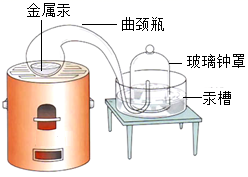 | | 密度 | 13.546g/cm3 | 密度 | 11.14g/cm3 | | 沸点 | 356.58°C | 不能溶于汞 | | 加热至沸与氧气反应,12天 | 分解温度 | 500°C | ① 写出汞与氧气反应的化学方程式。 ②拉瓦锡在实验中选择使用“汞”的优点如下: A 液态的汞在汞槽中既起到液封的作用,又能直接用来测见反应器内空间体积的变化。 B 汞加热后只跟氧气反应,且生成的氧化汞易加热分解又得到原先质量的汞和氧气,把得到的氧气加到剩下的4/5体积的气体中,结果所得气体跟空气的性质完全相同 C 氧化汞的密度小于汞,且不溶于汞,因此易与汞分离。 D 汞的沸点低,汞蒸气与氧气反应比较充分,能将密闭装置内空气中的氧气几乎耗尽。 但现在实验室的模仿研究却不用“汞”的原因有:。 ③加热红色氧化汞粉末得到汞和氧气的微观过程如下: 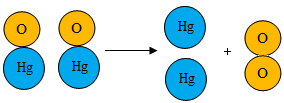 根据图示获得的信息是。 A 可说明分子质量大,原子质量小 B 可说明原子也能保持物质的化学性质 C 氧化汞由一个汞原子和一个氧原子构成 D 所得氧气与原空气中的氧气化学性质相同 |