【制备研究】 将金属钠与液态氨反应得NaNH2 , 再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O═NaN3+NaOH+X,X气体的化学式. 【Na2CO3质量分数测定】 工业级NaN3中常含有少量的Na2CO3 , 为测定样品中Na2CO3的质量分数设计如图1装置. (已知H2SO4溶液与NaN3 , 反应不生成气体.与碳酸钠反应生成二氧化碳气体). 提示:碱石灰是NaOH和CaO固体,能吸水和二氧化碳气体,氢氧化钠与二氧化碳反应生成碳酸和水. 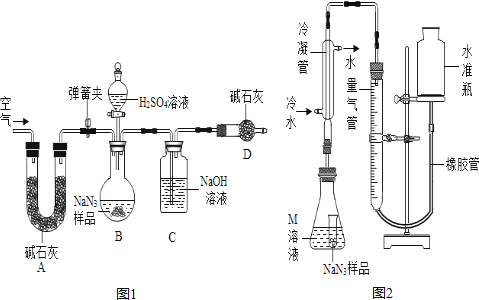
|